近日,毛颖基博士课题组研究发现,负载骨髓间充质干细胞(BMSCs)和神经干细胞(NSCs)的3D甲基丙烯酸酯明胶(GelMA)水凝胶功能支架植入大鼠脊髓半切处,可显著促进运动功能的恢复和神经元分化、减少胶质瘢痕、纤维化瘢痕和炎症反应。相关研究结果以“Promoting 3D neuronal differentiation in hydrogel for spinal cord regeneration”为题在线发表在Colloids and Surfaces B: Biointerfaces (中科院Top期刊)。

图1实验示意图。
脊髓损伤(SCI)治疗是如今难以攻克的世界性医学难题,细胞移植是目前SCI治疗的常用方法之一,但单一的细胞治疗效果并不理想,而组织工程治疗已成为未来的发展趋势。神经干细胞(NSCs)是一种多能干细胞,具有分化为神经元、少突胶质细胞和星形胶质细胞的能力。但实验研究证明,体内移植的NSCs主要分化为星形胶质细胞而不是神经元。骨髓间充质干细胞(BMSCs)不仅能抑制瘢痕组织和囊腔的形成,还能稳定轴突以及促进M1型巨噬细胞向M2型巨噬细胞的转化。这一过程可减少急性期的炎症反应,促进SCI修复。重要的是,BMSCs与NSCs共培养可促进NSCs向神经元的分化。然而,细胞直接移植到SCI部位,不仅会导致细胞的大量丢失,还可能由于损伤部位的缺血和炎症微环境导致移植细胞的死亡。更重要的是,移植NSCs的分化是不可控的。3D GelMA水凝胶因其优异的理化性质,具有模拟脊髓生理微环境、维持NSCs的存活和分化,同时还具有抗炎作用。
本研究通过组织工程的方式,用GelMA水凝胶对BMSCs和NSCs进行光固化,在体外通过调节水凝胶的浓度来模拟脊髓的结构和力学性能,促进NSCs向神经元分化,减少星形胶质细胞的形成。在体内,负载BMSCs和NSCs的3D水凝胶支架植入大鼠脊髓半切模型,更可有效促进SCI大鼠的运动功能恢复。
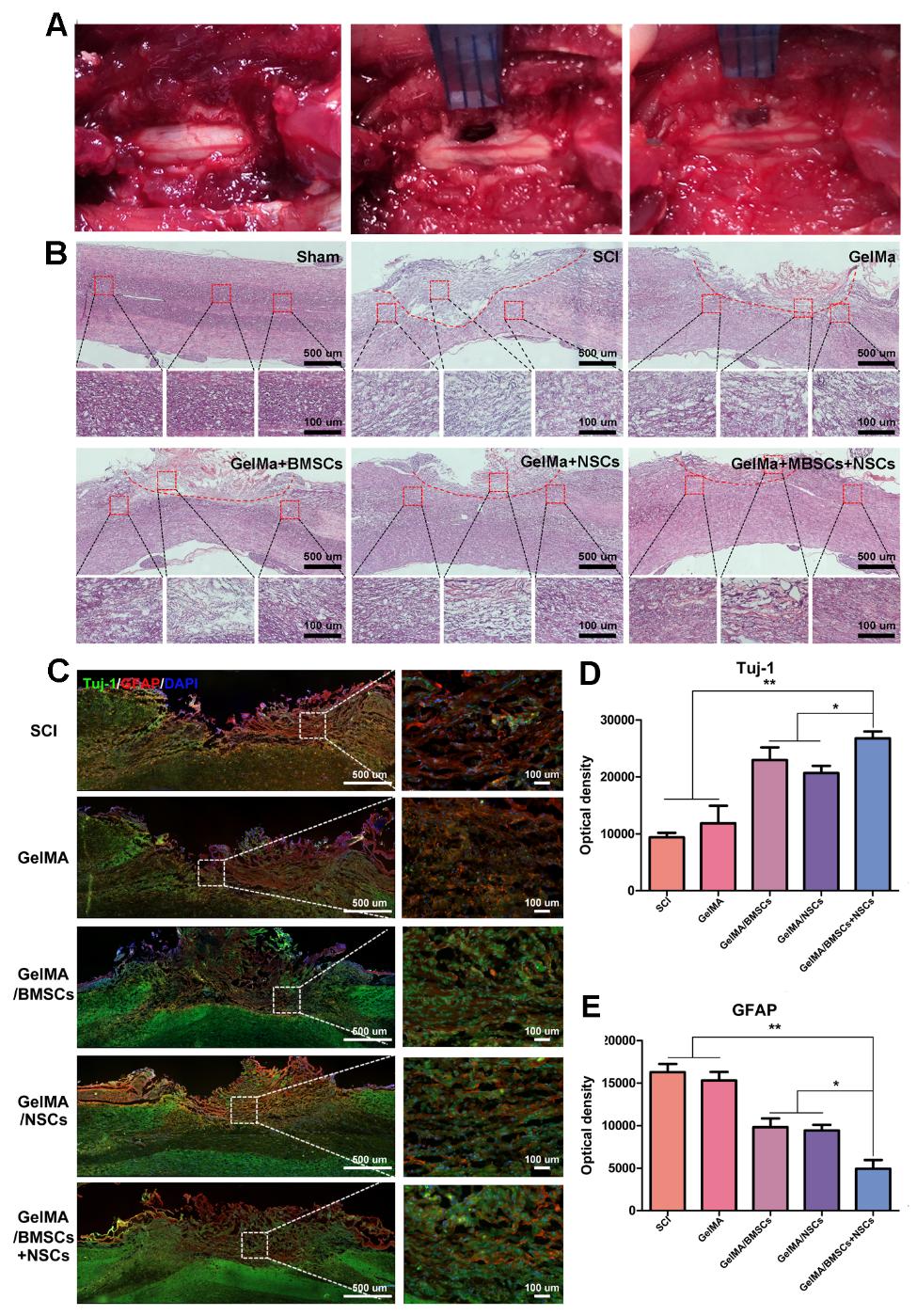
图2 负载BMSCs和NSCs的3 D GelMA水凝胶修复脊髓损伤
周平辉博士和2018级硕士生许盼盼为该论文共同第一作者,毛颖基博士和胡建国教授为论文共同通讯作者。该研究工作得到了国家自然科学基金、安徽省自然科学基金、蚌埠医学院骨科创新团队等项目资助。
论文链接:https://doi.org/10.1016/j.colsurfb.2020.111214
简介:毛颖基,博士、讲师,2017年11月毕业于中国科学技术大学/中国科学院合肥物质科学研究院,同年就职于蚌埠医学院生命科学学院生物技术教研室,主要研究方向:骨缺损、椎间盘退变及脊髓损伤等修复的组织工程研究。主持省自然、省教育厅、校转化医学和校科技发展基金项目各1项,以第一作者/通讯作者在Expert Opin Drug Del、Adv Wound Care、Colloid Surface B、Front Pant Sci、Iin Crop Prod等发表SCI 8篇。 (韩力/审 梁猛、毛颖基、许盼盼/文)